[ad_1]
Population d’étude
Il s’agissait d’un essai de luminothérapie clinique contrôlé par placebo randomisé chez les patients atteints de MP. Tous les participants ont été recrutés via des réseaux et des médias sociaux. L’approbation de l’éthique a été obtenue auprès du comité d’éthique de l’hôpital et a été enregistrée auprès de ClinicalTrials.gov (ClinicalTrials: NCT06129942, Date d’inscription: 12 novembre 2023, Registre des essais cliniques: le deuxième hôpital affilié de l’Université Soochow). Tous les participants ont donné un consentement éclairé écrit conformément à la Déclaration d’Helsinki.
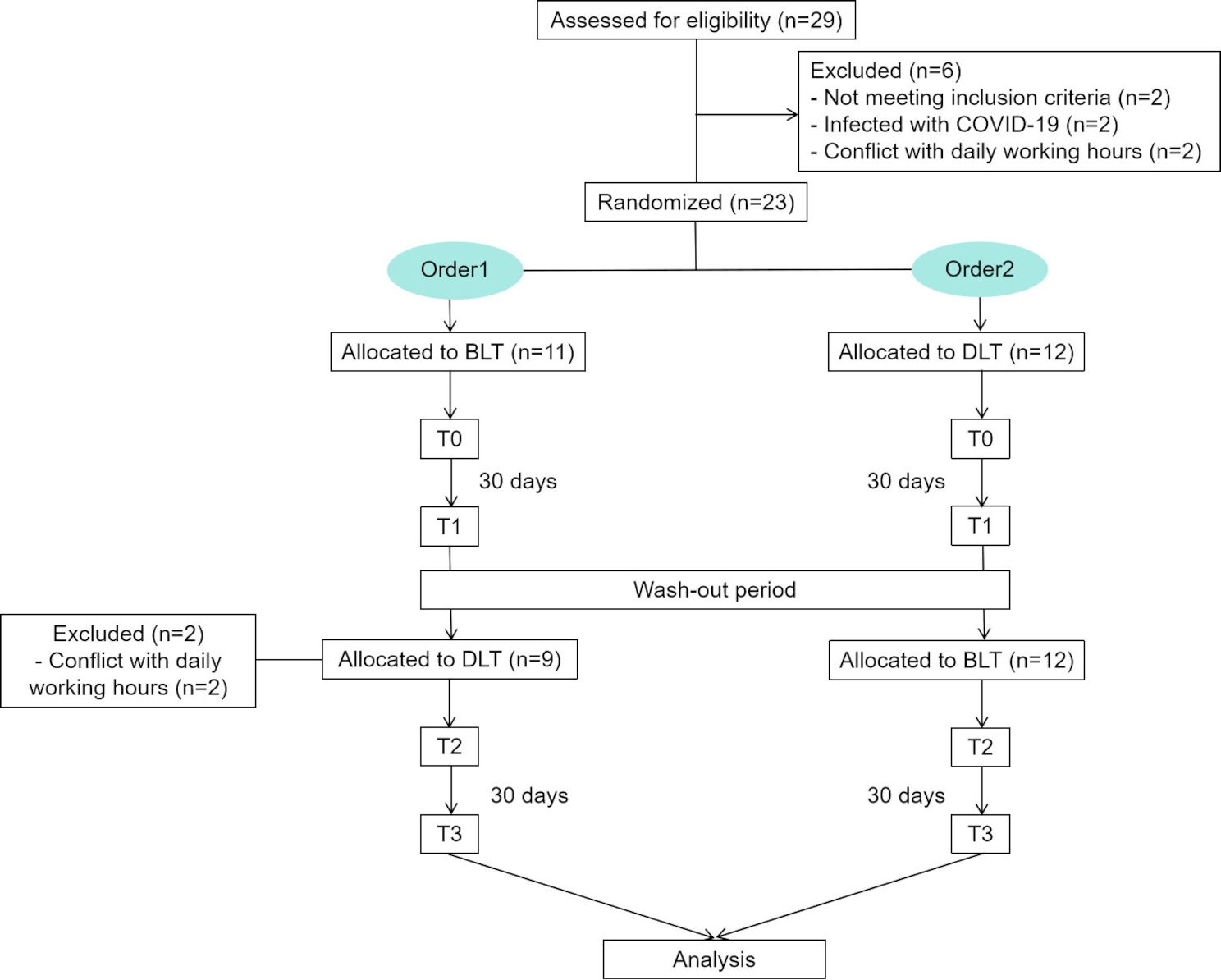
Vingt-neuf patients ont été recrutés entre septembre 2022 et septembre 2023 au sein de l’unité de troubles du mouvement du deuxième hôpital affilié de l’Université Soochow. Aucun changement de médicament ne s’est produit tout au long de l’étude.
Les patients ont été inscrits à l’étude s’ils (1) avaient un diagnostic de MP idiopathique, tel que défini par les critères de diagnostic clinique de la Société des troubles du mouvement de 2015 [13]; (2) ont été classés selon les étapes de Hoehn et Yahr (H&Y) 1 à 3; (3) a eu un régime de médicaments PD stable pendant au moins 6 mois avant le dépistage; et (4) étaient disposés et capables de donner un consentement éclairé écrit.
Les patients inscrits ont été exclus de cette étude s’ils (1) avaient le syndrome de parkinsonien atypique; (2) avaient des hallucinations ou une psychose non traitées; (3) avaient des maladies visuelles qui peuvent interférer avec une intervention légère, comme des cataractes sévères ou de la cécité; (4) parcouru 2 fuseaux horaires ou plus dans les 90 jours avant le dépistage de l’étude; (5) Avait du diabète sucré, une mauvaise stabilité assis, avait des antécédents de perte visuelle sévère, notamment la cataracte, le glaucome, la dégénérescence maculaire liée à l’âge, l’hypermyopie (dioptère réfractif> – 4.0d), ou tout autre historique de chirurgie oculaire.
Conception de l’étude
Les patients inscrits ont été randomisés pour commander 1 ou 2, en utilisant un calendrier de randomisation généré par ordinateur.
Lors de la visite de dépistage (T0), les participants inscrits à cette étude ont subi des évaluations ophtalmologiques et cliniques standard, notamment les stades de Hoehn et Yahr, la durée de la maladie, des doses équivalentes de la lévodopa selon Tomlinson et al. [14]qui ont tous été évalués à l’état «sur». Après la phase de référence, les participants ont ensuite été randomisés pour commander 1 ou l’ordre 2. À chaque période, les participants ont reçu 2 h de BLT (10000 lx) ou une luminothérapie DIM (DLT) (200 lx, comme thérapie lumineuse placebo) [10] À environ 45 degrés d’angle par rapport à la direction du regard (pour minimiser les effets secondaires de la lumière vive) le matin (une heure de 9 à 11h) et l’après-midi (une heure de 17h à 19h) par jour pendant 30 jours. La procédure LT a été signalée dans notre étude précédente [15].
Nous avons précédemment prouvé qu’après 14 jours de LT, l’effet a presque disparu [16]. Après une intervention de 30 jours, les participants ont connu une période de lavage de 30 jours, puis ont commencé l’intervention suivante. Les examens des ci-dessus ont également été effectués à trois autres étapes: fin du premier LT (T1), fin de la période de lavage (T2) et fin de la deuxième intervention (T3).
Évaluations cliniques
Évaluations cliniques chez tous les patients atteints de MP, y compris le stade Hoehn et Yahr, Durée de la maladie, révision parrainée par la société des troubles du mouvement des échelles unifiées de la maladie de Parkinson I-III (MDS-Updrs I-III) [17]Questionnaire de la maladie de Parkinson-39 (PDQ-39) [18]Échelle de gravité de la fatigue (FSS) [19] et questionnaire sur les symptômes non moteurs (NMSQ) [20] ont été menés dans tous les participants. La fonction cognitive a été évaluée par l’échelle d’évaluation cognitive de Montréal (MOCA) [21] échelle. La qualité subjective du sommeil a été évaluée par l’indice de qualité du sommeil de Pittsburgh (PSQI) [22]Échelle de somnolence Epworth (ESS) [23] et la 2e version de la maladie de la maladie de Parkinson (PDSS-2) [24] Balance. Le dysfonctionnement autonome a été évalué par l’échelle autonome des résultats dans la maladie de Parkinson (Scopa-Aut) [25] échelle. Le statut d’émotion a été évalué par une échelle de dépression de 24 éléments-Hamilton (HAMD-24) [26]et l’échelle d’anxiété de Hamilton à 14 éléments (HAMA-14) [27] Balance. RBD a été évalué par le questionnaire RBD Kong (RBDQ-HK) [28] échelle. Un neurologue qui était aveuglé à cette étude a effectué l’évaluation.
Examen OCT à haute définition
Nous avons utilisé OCT à haute définition (Cirrus HD-OCT, Carl Zeiss Meditec, Inc., Dublin, CA) chez tous les patients pour mesurer l’épaisseur de RNFL comme indiqué précédemment [9, 29]. L’épaisseur RNFL a été évaluée à l’aide d’un scanning de disque optique 200 × 200. Ce protocole a analysé un 6 mm2– Cube spatial basé entourant le disque optique et effectue 200 × 200-scans A dans environ 1,5 s. Le disque optique a acquis 200 B-scans avec 200 A-scans par B-scan (40 000 points). L’épaisseur de RNFL temporelle, nasale, supérieure et inférieure a été mesurée dans chaque œil et nous avons calculé le RNFL moyen.
Examen Perg
Perg (Visual Electrophysiologic Test Instrument, MKWHBMD, Medconova, Huzhou, China) a été obtenu en utilisant un dispositif de neurophysiologie pour le disque ERG (neuronique) et suivant la Société internationale pour l’électrophysiologie clinique de la vision (ISCEV) [30]. Les stimuli étaient des motifs en damier avec une taille de contrôle de 30 min d’angle visuel (arc min; contraste 90%; luminance moyenne, 93 cd / m2). Chaque Perg comprenait au moins deux essais. Les paramètres évalués étaient les latences P35, N95 et P50 (MS) et les amplitudes.
Examen VEP
Les examens VEP ont été traités par un système d’électromyographie intégratif (Keypoint.net, Danemark) dans la bascule de modèle Tessellated. Les participants étaient assis dans un environnement sombre et calme et ont été invités à prêter attention à l’écran. L’œil évalué était à 100 cm de l’écran et au même niveau. Les deux yeux ont été examinés séparément, avec un œil couvert tandis que l’autre a été examiné. Selon le système international d’électroencéphalogramme (EEG) 10/20, l’électrode d’enregistrement a été placée dans OZ, l’électrode de référence a été placée dans FPZ, la taille de la grille en damier était de 12/16 latences (MS).
Analyse statistique
L’analyse statistique a été effectuée avec le logiciel SPSS 26.0 et R. Les données ont été rapportées comme moyennes et SD ou médianes et interquartiles (IQR). Nous avons utilisé des échantillons appariés au test de rang signé Wilcoxon pour comparer les paramètres OCT, PERG et VEP et les scores d’échelle avant et après BLT ou DLT. La différence des valeurs et des paramètres des échelles avant et après LT et exprimés en paramètres ΔOCT, ΔPERG et ΔVEP. Les modèles de régression à effets mixtes ont ensuite été utilisés pour explorer s’il y avait un effet entre les deux interventions sur l’amélioration des différentiels des échelles, les paramètres OCT, PERG et VEP. Dans notre modèle linéaire mixte, les valeurs ΔScales, les paramètres ΔOCT, ΔPERG et ΔVEP étaient les variables dépendantes, et le type d’intervention était la variable indépendante. L’ordre, le stade, l’âge, le sexe, le H&Y, la LED et la durée de la maladie étaient des covariables, tandis que le participant a été un effet aléatoire. Les corrélations entre les paramètres ΔVep et ΔPerg et les valeurs de ΔScales ont été évaluées en utilisant ρ de Spearman non paramétrique. Un niveau de signification de P<0,05 a été utilisé pour tous les tests.
[ad_2]


